Uma solução é uma mistura homogênea de duas ou mais substâncias. Como, por exemplo, uma solução de sal (soluto) dissolvida em água (solvente).
 No dia a dia, várias vezes, até sem perceber, realizamos o processo de diluição de soluções. Por exemplo, a embalagem de produtos de limpeza e higiene doméstica, como desinfetantes, orienta que eles sejam diluídos antes de sua utilização. Alguns fabricantes sugerem nos rótulos do produto que ele seja diluído em água na proporção de 1 para 3, ou seja, para cada parte do produto, devem-se acrescentar 3 partes de água. Isso é feito, pois o produto é muito concentrado e forte, podendo danificar o local onde será aplicado se não for diluído da maneira certa. Por outro lado, se diluir mais do que deveria, pode-se perder dinheiro, porque o produto não atingirá o resultado desejado.
No dia a dia, várias vezes, até sem perceber, realizamos o processo de diluição de soluções. Por exemplo, a embalagem de produtos de limpeza e higiene doméstica, como desinfetantes, orienta que eles sejam diluídos antes de sua utilização. Alguns fabricantes sugerem nos rótulos do produto que ele seja diluído em água na proporção de 1 para 3, ou seja, para cada parte do produto, devem-se acrescentar 3 partes de água. Isso é feito, pois o produto é muito concentrado e forte, podendo danificar o local onde será aplicado se não for diluído da maneira certa. Por outro lado, se diluir mais do que deveria, pode-se perder dinheiro, porque o produto não atingirá o resultado desejado.
 Outro exemplo é ao fazermos sucos. Os rótulos de muitos sucos concentrados indicam que um copo desse suco deve ser diluído ou misturado a 5 copos de água. Assim, o suco fica “mais fraco”, isto é, menos concentrado.
Outro exemplo é ao fazermos sucos. Os rótulos de muitos sucos concentrados indicam que um copo desse suco deve ser diluído ou misturado a 5 copos de água. Assim, o suco fica “mais fraco”, isto é, menos concentrado.
Imagine que se diluiu um suco desses em 3 L de água. Se a concentração inicial do suco era de 40g/L, significa que tinha uma massa de 40 g para cada litro do solvente. Mas como teremos 3 L, a massa será dividida por 3 e a concentração será então de aproximadamente 13, 33 g/L, ou 13 gramas para cada litro de solução. Porém, na solução inteira ainda permanece a massa do soluto de 40g.
O cálculo dessa nova concentração pode ser feito da seguinte maneira:
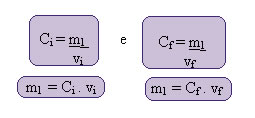
Onde os índices i e f representam, respectivamente, os valores iniciais e finais. Como o valor de m1 não mudou, podemos igualar as equações:
Ci . vi = Cf . vf
Substituindo os valores que temos, de acordo com o exemplo anterior, observe:
Solução inicial:
Ci: 40g/L
m1: 40g
vi: 1L
Solução final:
Cf: ?
m1: 40g
vf: 3L
Ci . vi = Cf . vf
(40 g/L) . (1 L) = Cf . 3L
Cf = 40 g /L
3
Cf = 13,333 g/L
O mesmo raciocínio é válido também para a concentração molar (M) e para a porcentagem em massa de soluto ou título (T):
Mi . vi = Mf . vf e Ti . vi = Tf . vf


Imagine que se diluiu um suco desses em 3 L de água. Se a concentração inicial do suco era de 40g/L, significa que tinha uma massa de 40 g para cada litro do solvente. Mas como teremos 3 L, a massa será dividida por 3 e a concentração será então de aproximadamente 13, 33 g/L, ou 13 gramas para cada litro de solução. Porém, na solução inteira ainda permanece a massa do soluto de 40g.
O cálculo dessa nova concentração pode ser feito da seguinte maneira:
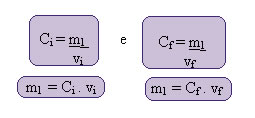
Onde os índices i e f representam, respectivamente, os valores iniciais e finais. Como o valor de m1 não mudou, podemos igualar as equações:
Ci . vi = Cf . vf
Substituindo os valores que temos, de acordo com o exemplo anterior, observe:
Solução inicial:
Ci: 40g/L
m1: 40g
vi: 1L
Solução final:
Cf: ?
m1: 40g
vf: 3L
Ci . vi = Cf . vf
(40 g/L) . (1 L) = Cf . 3L
Cf = 40 g /L
3
Cf = 13,333 g/L
O mesmo raciocínio é válido também para a concentração molar (M) e para a porcentagem em massa de soluto ou título (T):
Mi . vi = Mf . vf e Ti . vi = Tf . vf
Nenhum comentário:
Postar um comentário